| |
| Med Sci (Paris). 2007 November; 23(11): 1036–1038. Published online 2007 November 15. doi: 10.1051/medsci/200723111036.La vitamine A, loin des yeux… près du gras Isabelle Dugail* and Pascal Ferré* Inserm, U872, Paris, F-75006, France Centre de Recherche des Cordeliers, Université Pierre et Marie Curie, Paris 6, UMR S872, Paris, F-75006, France Université Paris Descartes, UMR S 872, Paris, F-75006, France Centre de recherche des cordeliers, Équipe 8, 15, rue de l’École de Médecine, 75006 Paris, France MeSH keywords: Adipocytes, Tissu adipeux, Glucides, Homéostasie, Humains, Lipides, Modèles biologiques, Rétinal, Rétinol |
Métabolisme de la vitamine A La vitamine A, ou rétinol, est un composé liposoluble apporté par l’alimentation, abondant dans le lait, les œufs, le foie et les huiles de poisson. Certains végétaux riches en β-carotènes (ou provitamine A) sont aussi des sources abondantes, mais une étape d’activation est alors nécessaire pour obtenir la vitamine. Des rôles multiples et complexes ont été décrits pour la vitamine A, dans la croissance cellulaire, la différenciation et la reproduction, mais son effet biologique « phare » (si l’on peut dire !) s’exerce au niveau de la rétine. La vitamine A est transformée en rétinal. Le rétinal s’associe à une protéine, l’opsine, pour former la rhodopsine présente dans les cellules photoréceptrices. Sous l’effet des photons, la structure du rétinal est modifiée et la rhodopsine change de conformation, ce qui induit, après un certain nombre d’étapes, le signal nerveux rétinien. Les carences en vitamine A, fréquentes en cas de malnutrition, sont une cause majeure de cécité dans les pays les plus pauvres.
 | Figure 1.
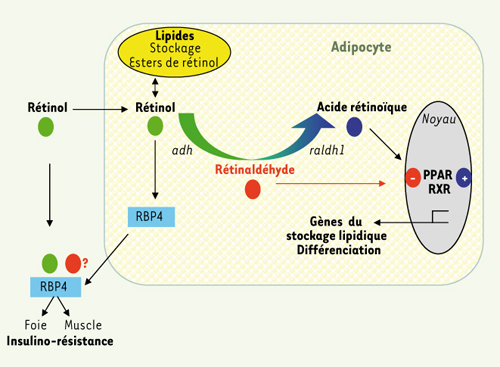
La vitamine A d’origine alimentaire est présente dans le plasma sous forme liée à une protéine de liaison RBP4. Dans le tissu adipeux, le rétinol peut être stocké sous forme d’esters dans les gouttelettes lipidiques, ou métabolisé en deux composés qui exercent des effets distincts sur l’expression des gènes du stockage lipidique. Le rétinaldéhyde inhibe la différenciation adipocytaire et le stockage, alors que l’acide rétinoïque est un activateur transcriptionnel du dimère PPAR-RXR. RBP4 est produite par les adipocytes et se comporte comme une adipokine qui diminue la sensibilité à l’insuline des tissus périphériques comme le foie et le muscle. L’équilibre intra-adipocytaire entre rétinaldéhyde/acide rétinoïque est déterminé par l’activité des enzymes de l’oxydation du rétinol : alcool-déshydrogénase (adh) et retinaldéhyde déshydrogénase 1 (raldh1). La liaison potentielle du rétinaldéhyde à RBP4 et ses conséquences délétères sur la sensibilité à l’insuline ne sont pas documentées. |
Le rétinol, hydrophobe, circule dans le compartiment sanguin conjugué à des protéines de transport comme les retinol binding protein (RBP). Au niveau intracellulaire, le rétinol est transformé en rétinaldéhyde par une alcool déshydrogénase puis en acide rétinoïque par la rétinaldéhyde déshydrogénase de type 1 (raldh1) [
1]. Les différents isomères de l’acide rétinoïque (9-cis et tout-trans) peuvent réguler la transcription de nombreux gènes car ils sont des ligands naturels des récepteurs nucléaires de la famille RAR (retinoic acid receptor) et RXR (retinoid X receptor). Le rétinol est stocké dans le foie mais également dans la gouttelette lipidique de l’adipocyte, sous forme d’esters. |
Rétinaldéhyde et développement du tissu adipeux Un article publié en mai 2007 dans la revue Nature Medicine [
2] démontre que le rétinaldéhyde exerce des effets spécifiques dans le développement du tissu adipeux et dans la régulation de l’homéostasie glucido-lipidique, distincts de ceux des isomères de l’acide rétinoïque. Les auteurs ont observé la présence de concentrations importantes de rétinaldéhyde (entre 100 nM et 1 µM) dans le tissu adipeux des rongeurs, ainsi que la régulation différentielle, au cours du processus de différenciation adipocytaire, des enzymes permettant la synthèse du rétinaldéhyde (à partir du rétinol) et son catabolisme (en acide rétinoique). Ils ont alors fait l’hypothèse d’un rôle spécifique du rétinaldéhyde dans la différenciation adipocytaire et donc dans le développement du tissu adipeux. Des études in vitro sur des lignées cellulaires ont montré en effet un effet inhibiteur du rétinaldéhyde sur la différenciation adipocytaire, indépendant de sa transformation en acide rétinoique. Les auteurs ont ensuite utilisé un modèle de souris invalidées pour le gène codant la rétinaldéhyde déshydrogénase de type 1 ce qui inhibe le catabolisme du rétinaldéhyde. Ces souris présentent des concentrations élevées de rétinaldéhyde plasmatique. In vitro, les fibroblastes embryonnaires des souris raldh1−/−
présentent une différenciation adipocytaire réduite, le rétinaldéhyde agissant en partie en inhibant l’activité transcriptionnelle du dimère RXR-PPARγ, le régulateur majeur de la différenciation des adipocytes. Le gain de poids des souris raldh1−/−
en réponse à un régime hyperlipidique riche en vitamine A est fortement réduit par rapport aux témoins, en raison du moindre développement des dépôts adipeux sous-cutanés et viscéraux. La taille des adipocytes est négativement corrélée aux concentrations tissulaires de rétinaldéhyde. Les souris raldh1−/−
ne présentent pas de diminution de la prise alimentaire, mais on observe chez ces animaux une augmentation des dépenses énergétiques. |
Rétinaldéhyde et homéostasie glucido-lipidique Il est désormais bien établi que le développement excessif du tissu adipeux influence l’homéostasie glucido-lipidique via la production d’adipokines qui modulent la sensibilité à l’insuline des tissus périphériques [
3]. Les souris raldh1−/−
qui résistent à l’obésité induite par un régime hyperlipidique ne développent pas non plus d’insulino-résistance en réponse à un régime riche en graisses, et produisent moins d’adipokines. Le rétinalhéhyde est spécifiquement responsable de ce phénotype puisque son administration améliore la tolérance au glucose de souris obèses insulino-résistantes alors que celle de rétinol ou d’acide rétinoique n’a aucun effet. Ainsi, ces résultats démontrent un rôle spécifique du rétinaldéhyde, distinct de celui de la vitamine A ou de l’acide rétinoïque, dans le métabolisme et le développement du tissu adipeux. Ils peuvent être mis en perspective avec d’autres travaux récents du groupe de B.B. Kahn [
4] qui avaient mis en évidence l’importance de la production adipocytaire d’une protéine de liaison du rétinol (retinol binding protein-4, RBP4) dans les désordres de l’homéostasie glucidique liés à l’obésité. Les propriétés métaboliques de la RBP4 avaient été découvertes à l’occasion du criblage des protéines spécifiquement produites par les adipocytes présentant un déficit d’expression pour le transporteur de glucose sensible à l’insuline Glut4, une anomalie caractéristique du diabète de type 2. L’injection de RBP4 recombinante ou sa surexpression dans des souris transgéniques induit une insulino-résistance périphérique (musculaire et hépatique), alors que l’invalidation du gène RBP4, ou l’administration d’un composé qui augmente son excrétion urinaire (la fenretinide, un rétinoïde de synthèse), améliore la tolérance au glucose des rongeurs diabétiques. Il est possible que la quantité de RBP4 module la disponibilité en rétinaldéhyde ce qui constituerait donc un nouveau signal d’origine adipocytaire agissant à distance sur la sensibilité à l’insuline des tissus périphériques. |
L’ensemble de ces travaux met en lumière des propriétés nouvelles pour les composés impliqués dans le métabolisme de la vitamine A. D’une part, le rétinaldéhyde limite le développement adipocytaire et favorise la dissipation de l’énergie, au moins chez le rongeur. D’autre part, la RBP4 apparaît comme un signal dépendant de l’utilisation de glucose et fortement associé à l’insulino-résistance. Bien que les relations potentielles entre le rétinaldéhyde et RBP4 restent encore à préciser, ces nouvelles découvertes pourraient constituer une voie d’intervention prometteuse pour le développement de stratégies thérapeutiques contre les maladies métaboliques de surcharge comme l’obésité et le diabète de type 2. |
1. Molotkov A, Duester G. Genetic evidence that retinaldehyde dehydrogenase Raldh1 (Aldh1a1) functions downstream of alcohol dehydrogenase Adh1 in metabolism of retinol to retinoic acid. J Biol Chem 2003; 278 : 36085–90. 2. Ziouzenkova O, Orasanu G, Sharlach M, et al. Retinaldehyde represses adipogenesis and diet-induced obesity. Nat Med 2007; 13 : 695–702. 3. Trujillo ME, Scherer PE. Adipose tissue-derived factors: impact on health and disease. Endocr Rev 2006; 27 : 762–78. 4. Yang Q, Graham TE, Mody N, Preitner F, et al. Serum retinol binding protein 4 contributes to insulin resistance in obesity and type 2 diabetes. Nature 2005; 436 : 356–62. |